اختلال در منابع انرژی و تنفس سلول، چه میکند؟
میوپاتی میتوکندریایی چیست؟
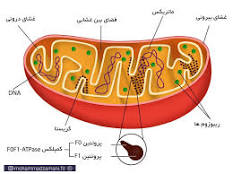
بیماریهای میتوکندری ناشی از نقص در میتوکندری است- که کارخانههای انرژی هستند و تقریباً در تمام سلولهای بدن یافت میشود. بیماریهای میتوکندریایی- که باعث مشکلات عضلانی برجسته میشوند- میوپاتی میتوکندریایی نامیده میشوند (میو به معنای ماهیچه و پاتوس به معنای بیماری است)، در حالی که بیماریهای میتوکندری- که باعث مشکلات عضلانی و عصبی برجسته میشوند- آنسفالومیوپاتی میتوکندری نامیده میشوند (انسفالو به مغز اشاره دارد).
یک سلول انسانی معمولی برای برآوردن نیازهای انرژی خود به صدها میتوکندری متکی است. علائم بیماری میتوکندری متفاوت است، زیرا یک فرد می تواند ترکیبی منحصر به فرد از میتوکندری سالم و معیوب، با توزیع منحصر به فرد در بدن داشته باشد. در بیشتر موارد، بیماری میتوکندری، یک اختلال چند سیستمی است که بیش از یک نوع سلول، بافت یا اندام را تحت تاثیر قرار می دهد.
چون سلولهای عضلانی و عصبی نیاز به انرژی بالایی دارند، مشکلات عضلانی و عصبی از ویژگیهای مشترک بیماری میتوکندری هستند.
سایر عوارض مکرر عبارتند از: اختلال در بینایی، آریتمی قلبی (ضربان غیر طبیعی قلب)، دیابت و توقف رشد.
معمولاً یک فرد مبتلا به بیماری میتوکندری، دارای دو یا چند مورد از این موارد است و برخی از آنها به قدری منظم با هم رخ می دهند که در دسته سندرم ها گروه بندی می شود.
میوپاتی:
علائم اصلی میوپاتی میتوکندری عبارتند از:
خستگی عضلانی
ضعف
عدم تحمل ورزش
شدت هر یک از این علائم از فردی به فرد دیگر حتی در یک خانواده بسیار متفاوت است.
در برخی افراد، ضعف در ماهیچه هایی که حرکات چشم و پلک را کنترل می کنند، بارزتر است. عواقب رایج عبارتند از فلج تدریجی حرکات چشم به نام افتالموپلژی خارجی پیشرونده (PEO) و افتادگی پلک های فوقانی که پتوز نامیده می شود. اغلب، افراد به طور خودکار PEO را با حرکت دادن سر خود برای نگاه کردن به جهات مختلف جبران می کنند و ممکن است متوجه هیچ مشکل بینایی نشوند.
پتوز می تواند بینایی را مختل کند و باعث بی حالی شود، اما می توان آن را با جراحی اصلاح کرد.
میوپاتی میتوکندریال همچنین می تواند باعث ضعف و تحلیل عضلات دیگر صورت و گردن شود و می تواند منجر به مشکل در بلع و به ندرت تکلم شود.
افراد مبتلا به میوپاتی میتوکندریال، ممکن است ضعف عضلانی در بازوها و پاهای خود را تجربه کنند.
عدم تحمل ورزش- که خستگی ناشی از فعالیت نیز نامیده می شود- به احساس خستگی غیرعادی ناشی از فعالیت بدنی اشاره دارد. درجه عدم تحمل ورزش در بین افراد، بسیار متفاوت است. برخی افراد ممکن است فقط با فعالیت های ورزشی مانند دویدن، مشکل داشته باشند، در حالی که برخی دیگر ممکن است در فعالیت های روزمره مانند راه رفتن به سمت صندوق پست یا بلند کردن جعبه ی شیر دچار مشکل شوند.
گاهی، بیماری میتوکندریال با گرفتگی عضلات همراه است. در موارد نادری میتواند منجر به تحلیل عضلات و درد بعد از ورزش شود. این تجزیه، باعث نشت پروتئینی به نام میوگلوبین از ماهیچه ها به داخل ادرار (میوگلوبینوری) می شود. گرفتگی یا میوگلوبینوری معمولاً زمانی اتفاق میافتد که فرد مبتلا به عدم تحمل ورزش، «بیش از حد آن را انجام دهد» و میتواند در طول فعالیت بیش از حد یا چندین ساعت پس از آن رخ دهد.
در حالی که باید از فعالیت بیش از حد اجتناب شود، به نظر می رسد ورزش متوسط، به افراد مبتلا به میوپاتی میتوکندری کمک می کند تا قدرت خود را حفظ کنند.
آنسفالومیوپاتی:
انسفالومیوپاتی میتوکندریال معمولاً شامل برخی از علائم میوپاتی به اضافه یک یا چند علامت عصبی است. این علائم در بین افراد از نظر نوع و شدت بسیار متفاوت است.
انسفالومیوپاتی میتوکندریال علاوه بر تأثیر بر عضلات چشم، می تواند خود چشم و بخش هایی از مغز را- که در بینایی نقش دارند- تحت تأثیر قرار دهد. به عنوان مثال، از دست دادن بینایی، به دلیل آتروفی بینایی (کوچک شدن عصب بینایی) یا رتینوپاتی (دژنراسیون برخی از سلول های پشت چشم)، یکی از علائم رایج انسفالومیوپاتی میتوکندری است.
کم شنوایی حسی عصبی SNHL یکی از علائم شایع بیماری های میتوکندری است. علت آن، آسیب به گوش داخلی(حلزون گوش) یا عصب شنوایی است که گوش داخلی را به مغز متصل می کند. کم شنوایی حسی عصبی، دائمی است اما می توان آن را از طریق اشکال جایگزین ارتباط، سمعک یا کاشت حلزون کنترل کرد. سمعک صداها را قبل از رسیدن به گوش داخلی تقویت می کند. کاشت حلزون قسمت های آسیب دیده گوش داخلی را دور می زند و عصب شنوایی را تحریک می کند.
بیماریهای میتوکندری میتوانند باعث آتاکسیعدم تعادل شوند که به اختلال در تعادل و هماهنگی اشاره دارد. افراد مبتلا به آتاکسی، مستعد افتادن هستند و ممکن است نیاز به استفاده از وسایل کمکی مانند نرده، واکر یا ویلچر داشته باشند.
دکتر سید سلمان فاطمی . نورولوژیست, [5/10/2023 8:46 AM]
فیزیوتراپی و کاردرمانی ممکن است کمک کند.
سایر علائم رایج آنسفالومیوپاتی میتوکندری شامل سردردهای میگرنی و تشنج است. داروهای موثر بسیاری برای درمان و کمک به پیشگیری از میگرن و تشنج وجود دارد.
مسائل خاص در بیماری میتوکندری
مراقبت های تنفسی- بیماری های میتوکندریال می توانند بر عضلات یا قسمت هایی از مغز- که از تنفس پشتیبانی می کنند- تأثیر بگذارند. فردی با مشکلات تنفسی خفیف ممکن است نیاز به حمایت های تنفسی گاه به گاه مانند هوای تحت فشار داشته باشد. فردی که مشکلات شدیدتری دارد ممکن است نیاز به حمایت دائمی از یک دستگاه تنفس مصنوعی داشته باشد. افراد باید مراقب علائم و مشکلات تنفسی (مانند تنگی نفس یا سردردهای صبحگاهی) باشند و به طور منظم توسط متخصص تنفس معاینه شوند.
مراقبت از قلب: برخی از بیماری های میتوکندری می توانند باعث کاردیومیوپاتی (ضعف عضله قلب) یا آریتمی (ضربان قلب نامنظم) شوند. اگرچه آریتمی قلبی خطرناک است، اما با ضربانساز، قابل درمان است. افراد مبتلا به اختلالات میتوکندری ممکن است نیاز به معاینات منظم توسط متخصص قلب داشته باشند.
سایر مشکلات سلامتی بالقوه - افراد مبتلا به بیماری میتوکندری ممکن است مشکلات گوارشی، دیابت و/یا مشکلات کلیوی را تجربه کنند. برخی از این مشکلات اثرات مستقیم نقص میتوکندری در سیستم گوارش، لوزالمعده (در دیابت) یا کلیه ها و برخی دیگر اثرات غیرمستقیم نقص میتوکندری در سایر بافت ها هستند. به عنوان مثال، میوگلوبینوری بر توانایی کلیه ها برای فیلتر کردن مواد زائد از خون تاکید می کند و می تواند باعث آسیب کلیه شود.
مسائل مورد توجه ویژه در کودکان:
بینایی - اگرچه فلج تدریجی حرکات چشم (PEO) و پتوز معمولاً فقط باعث اختلال خفیف بینایی در بزرگسالان می شود، اما به طور بالقوه در کودکان مبتلا به میوپاتی میتوکندری مضرتر هستند. چون رشد مغز به تجربیات دوران کودکی حساس است، PEO یا پتوز در دوران کودکی می تواند باعث آسیب دائمی به سیستم بینایی مغز شود. برای کودکان دارای علائم PEO یا پتوز مهم است که بینایی خود را توسط متخصص بررسی کنند.
تأخیر در رشد - به دلیل ضعف عضلانی، ناهنجاری های مغزی یا ترکیبی از هر دو، کودکان مبتلا به بیماری های میتوکندری ممکن است در رشد مهارت های خاصی دچار مشکل شوند. برای مثال، ممکن است زمان زیادی طول بکشد تا به نقاط عطف حرکتی مانند نشستن، خزیدن و راه رفتن برسند. همانطور که بزرگتر می شوند، ممکن است نتوانند به راحتی مانند سایر کودکان هم سن و سال خود رفت و آمد کنند و ممکن است مشکلات گفتاری و/یا اختلالات یادگیری داشته باشند. کودکانی که تحت تأثیر این مشکلات قرار می گیرند ممکن است از مداخلات اولیه و خدماتی مانند درمان فیزیکی و گفتار درمانی و احتمالاً یک برنامه آموزشی فردی در مدرسه بهره مند شوند.
چه کسانی بیشتر در معرض ابتلا به میوپاتی میتوکندری هستند؟
بیماری های میتوکندری در اثر جهش های ژنتیکی ایجاد می شوند. ژنها دستورالعملهای ساخت پروتئینها را ارائه میکنند و ژنهای درگیر در بیماری میتوکندری معمولاً پروتئینهایی را میسازند که در داخل میتوکندری کار میکنند. در داخل هر میتوکندری، این پروتئینها بخشی از خط مونتاژی را تشکیل میدهد که از مولکولهای سوخت (قند و چربی) مشتق شده و از غذا همراه با اکسیژن برای تولید مولکول انرژی آدنوزین تری فسفات یا ATP استفاده میکند.
پروتئین ها در ابتدای خط مونتاژ، قند و چربی را وارد میتوکندری می کنند و سپس آنها را برای تامین انرژی تجزیه می کنند و از این انرژی برای ساخت ATP استفاده میکنند. این بخش بسیار کارآمد از فرآیند تولید ATP، به اکسیژن نیاز دارد و زنجیره ی تنفسی نامیده می شود.
یک سلول پر از میتوکندری معیوب، از ATP محروم میشود و میتواند مقداری از مولکولهای سوخت استفاده نشده و اشکال مخرب اکسیژن به نام رادیکالهای آزاد یا گونههای اکسیژن فعال را در خود جمع کند. اینها ترکیبات آنتی اکسیدانی (موجود در بسیاری از غذاها و مکمل های غذایی)، به نظر می رسد دفاعی کلی در برابر پیری و بیماری ارائه می دهند.
در چنین مواردی، مولکولهای سوخت اضافی برای ساخت ATP از روشهای ناکارآمد استفاده میکنند که میتواند محصولات جانبی بالقوه مضری مانند اسید لاکتیک تولید کند. (این همچنین زمانی اتفاق میافتد که یک سلول، اکسیژن کافی نداشته باشد. این حالت میتواند در طول ورزش شدید برای سلولهای ماهیچهای اتفاق بیفتد.)
تجمع اسید لاکتیک در خون - که اسیدوز لاکتیک نامیده میشود - با خستگی عضلانی مرتبط است و ممکن است به بافت عضلانی و عصبی آسیب برساند.
سلول های عضلانی و عصبی از ATP مشتق شده از میتوکندری، به عنوان منبع اصلی انرژی خود استفاده می کنند. اثرات ترکیبی کمبود انرژی و تجمع سم در این سلول ها می تواند منجر به بسیاری از علائم عضلانی و عصبی شود.
وراثت:
وراثت بیماریهای میتوکندری پیچیده است و اغلب ردیابی میوپاتی میتوکندری از طریق یک شجره نامه، دشوار است. در واقع، بسیاری از موارد بیماری میتوکندری، پراکنده هستند، به این معنی که بدون هیچ سابقه ی خانوادگی، رخ می دهند.
برای درک چگونگی ارث بیماری های میتوکندری، مهم است که بدانید دو نوع ژن ضروری برای میتوکندری وجود دارد. نوع اول در داخل هسته ی سلول قرار دارد. این هسته محفظه ای در سلول های ما حاوی بیشتر مواد ژنتیکی یا DNA است. نوع دوم منحصراً در DNA موجود در میتوکندری قرار دارد.
جهش در DNA هسته ای (nDNA) یا DNA میتوکندریایی (mtDNA) می تواند باعث بیماری میتوکندری شود.
خطر انتقال بیماری میتوکندری به کودک به عوامل زیادی بستگی دارد، از جمله اینکه آیا این بیماری به دلیل جهش در nDNA یا mtDNA ایجاد می شود.
برخی از سندرم های مرتبط با بیماری میتوکندری عبارتند از:
شروع سندرم بارثBarth : ویژگی های دوران نوزادی: علائم معمولی شامل کاردیومیوپاتی، ضعف عمومی عضلانی و تعداد کم گلبول های سفید خون است که منجر به افزایش خطر عفونت می شود. این سندرم زمانی در دوران نوزادی به طور یکنواخت کشنده در نظر گرفته می شد، اما برخی افراد اکنون بسیار طولانی تر زندگی می کنند.
افتالموپلژی خارجی پیشرونده مزمن (cPEO)
شروع: معمولاً در نوجوانی یا اوایل بزرگسالی
ویژگی ها: PEO اغلب علامت بیماری میتوکندری است. در برخی افراد، این یک بیماری مزمن و به آرامی پیشرونده است که با بی ثباتی حرکت چشم ها و ضعف عمومی و عدم تحمل ورزش همراه است.
شروع سندرم Kearns-Sayre (KSS)
: قبل از 20 سالگی
ویژگی ها: PEO (معمولاً به عنوان علامت اولیه) و رتینوپاتی رنگدانه، یک رنگدانه نمک و فلفل در شبکیه چشم که می تواند بینایی را تحت تاثیر قرار دهد.
سایر علائم رایج شامل کاردیومیوپاتی، بلوک هدایت (نوعی آریتمی قلبی) آتاکسی، کوتاهی قد، نوروپاتی و ناشنوایی است.
سندرم لی leigh (MILS یا سندرم لی ارثی مادر)
شروع: در دوران نوزادی یا اوایل کودکی
ویژگی ها: ناهنجاری های مغزی که می تواند منجر به تون ماهیچه های غیر طبیعی، آتاکسی، تشنج، اختلال در بینایی و شنوایی، تاخیر در رشد و مشکلات تنفسی شود. نوزادان مبتلا به این بیماری پیش آگهی بدی دارند.
سندرم های کاهش DNA میتوکندریایی (MDDS)
شروع: در دوران نوزادی
ویژگی ها: شکل میوپاتیک MDDS، با ضعف مشخص می شود که در نهایت بر عضلات تنفسی تأثیر می گذارد. برخی از اشکال MDDS، مانند سندرم آلپر، با ناهنجاری های مغزی و بیماری کبدی پیشرونده مشخص می شوند. داروی ضد تشنج سدیم والپروات باید در کودکان مبتلا به سندرم آلپر alpers با احتیاط مصرف شود زیرا می تواند خطر نارسایی کبدی را افزایش دهد.
انسفالومیوپاتی میتوکندری، اسیدوز لاکتیک و اپیزودهای شبه سکته مغزی (MELAS)
شروع: از کودکی تا اوایل بزرگسالی
ویژگیها: علائم MELAS انسفالومیوپاتی همراه با تشنج و/یا زوال عقل، اسیدوز لاکتیک و دورههای مکرر شبیه سکته ی مغزی است. این دورهها سکتههای معمولی نیستند، که وقفههایی در جریان خون مغز هستند که باعث علائم عصبی ناگهانی میشوند. با این حال، این اپیزودها می توانند در کوتاه مدت علائمی شبیه به سکته ی مغزی ایجاد کنند (مانند از دست دادن موقت بینایی، مشکل در صحبت کردن، یا مشکل در درک گفتار) و منجر به آسیب مغزی پیشرونده شوند. علت اپیزودهای سکته مانند نامشخص است.
انسفالومیوپاتی عصبی میتوکندریایی گوارشی (MNGIE)
شروع: معمولاً قبل از 20 سالگی
ویژگی ها: این اختلال با PEO، پتوز، ضعف اندام و مشکلات گوارشی (هضم) از جمله استفراغ، اسهال مزمن و درد شکمی مشخص می شود. یکی دیگر از علائم رایج، نوروپاتی محیطی است (یک اختلال در عملکرد اعصاب که می تواند منجر به اختلال حسی و ضعف عضلانی شود).
صرع میوکلونوس با الیاف قرمز پاره شده (MERRF)
شروع: اواخر کودکی تا نوجوانی
ویژگی ها: بارزترین علائم MERRF عبارتند از میوکلونوس (تکان های عضلانی)، تشنج، آتاکسی و ضعف عضلانی. این بیماری همچنین می تواند باعث کاهش شنوایی و کوتاهی قد شود.
نوروپاتی، آتاکسی و رتینیت پیگمانتوزا (NARP)
شروع: از نوزادی تا بزرگسالی
ویژگی ها: NARP توسط یک جهش mtDNA ایجاد می شود که به MILS نیز مرتبط است و این دو سندرم می توانند در یک خانواده رخ دهند. NARP علاوه بر علائم اصلی که برای آنها نامگذاری شده است، می تواند شامل تاخیر رشد، تشنج و زوال عقل باشد. (رتینیت پیگمانتوزا به تخریب شبکیه ی چشم و در نتیجه از دست دادن بینایی اشاره دارد.)
سندرم پیرسون:
ویژگی های دوران نوزادی: این سندرم شامل کم خونی شدید و اختلال در عملکرد پانکراس است. کودکان مبتلا به این بیماری معمولاً به سندرم کرنز-سایر مبتلا می شوند.
میوپاتی میتوکندریایی چگونه تشخیص داده و درمان می شود؟
تشخیص میوپاتی میتوکندریایی
تشخیص میوپاتی میتوکندری به طور کلی شامل موارد زیر است:
ارزیابی سابقه پزشکی و خانوادگی.
دکتر سید سلمان فاطمی . نورولوژیست, [5/10/2023 8:46 AM]
معاینات فیزیکی و عصبی. معاینه فیزیکی معمولاً شامل تستهای قدرت و استقامت است، مانند تست ورزش (که میتواند شامل فعالیتهایی مانند مشت کردن مکرر باشد). معاینه عصبی می تواند شامل تست های رفلکس، بینایی، گفتار و مهارت های اساسی شناختی (تفکر) باشد.
آزمایشات آزمایشگاهی برای بررسی دیابت، مشکلات کبدی و کلیوی و افزایش اسید لاکتیک در خون و ادرار. برخی موارد ممکن است نیاز به اندازه گیری اسید لاکتیک در مایع مغزی نخاعی (CSF) داشته باشد که فضاهای داخل مغز و نخاع را پر می کند. اندازهگیری را میتوان با جمعآوری مایع مغزی نخاعی از طریق شیر نخاعی انجام داد، یا با طیفسنجی MR - تکنیکی- که از سیگنال MRI برای تشخیص تغییرات در سطح اسید لاکتیک و سایر مواد شیمیایی در مغز استفاده میکند- تخمین زد.
الکتروکاردیوگرام (EKG) برای بررسی قلب برای علائم آریتمی و کاردیومیوپاتی.
تصویربرداری تشخیصی، مانند توموگرافی کامپیوتری (CT) یا تصویربرداری رزونانس مغناطیسی (MRI) برای بررسی مغز برای ناهنجاریهای رشدی یا علائم آسیب. تشنج با نوار مغز مشخص میشود.
نهایتا بیوپسی عضلانی، که شامل برداشتن و بررسی نمونه ی کوچکی از بافت عضلانی است. هنگامی که با رنگی که میتوکندری را به رنگ قرمز رنگ میکند، پرداخت میشود، ماهیچههایی که تحت تأثیر بیماری میتوکندری قرار میگیرند، اغلب فیبرهای قرمز ناهموار را نشان میدهند.
سایر لکه ها می توانند عدم وجود آنزیم های ضروری میتوکندری را در عضله تشخیص دهند. همچنین می توان پروتئین های میتوکندری را از ماهیچه، استخراج کرد و فعالیت آنها را اندازه گیری کرد. از تکنیک های غیرتهاجمی مانند طیف سنجی MR می توان برای بررسی عضله بدون نمونه برداری از بافت استفاده کرد.
آزمایش ژنتیکی می تواند تعیین کند آیا فردی دارای جهش ژنتیکی است که باعث بیماری میتوکندری می شود یا خیر. در این آزمایشات از مواد ژنتیکی استخراج شده از خون یا نمونه برداری از عضله استفاده می شود. اگرچه یک نتیجه ی آزمایش مثبت، می تواند تشخیص اختلال میتوکندری را تأیید کند، اما تفسیر نتیجه ی آزمایش منفی می تواند دشوارتر باشد. این می تواند به این معنی باشد که یک فرد، دارای یک جهش ژنتیکی است که آزمایش قادر به تشخیص آن نیست.
درمان میوپاتی میتوکندریایی:
اگرچه درمان خاصی برای هیچ یک از میوپاتی های میتوکندری وجود ندارد، فیزیوتراپی ممکن است دامنه حرکت عضلات را افزایش داده و مهارت را بهبود بخشد.
بهجای تمرکز بر عوارض خاص بیماری میتوکندری، برخی از درمانهای تحت بررسی به رفع یا دور زدن میتوکندری معیوب میپردازند. این درمانها مکملهای تغذیهای هستند که بر پایه سه ماده طبیعی دخیل در تولید ATP در سلولهای ما هستند - کراتین، کارنیتین و کوآنزیم Q10 (همچنین به عنوان CoQ10 یا ubiquinone نیز شناخته میشود).
دانشمندان در حال بررسی مزایای احتمالی برنامه های ورزشی و مکمل های غذایی، عمدتاً نسخه های طبیعی و مصنوعی CoQ10 هستند. در حالی که CoQ10 برای کمبود اولیه CoQ10 مفید است، مشخص نیست که آیا سایر مکملهای غذایی برای درمان بیماریهای میتوکندری مفید هستند یا خیر.
دانشمندان بسیاری از جهش های ژنتیکی را که باعث بیماری های میتوکندری می شوند، شناسایی کرده اند. آنها از این دانش برای ایجاد مدل های حیوانی بیماری میتوکندری استفاده کرده اند که می تواند برای بررسی درمان های بالقوه مورد استفاده قرار گیرد. دانشمندان همچنین آزمایشهای ژنتیکی طراحی کردهاند که امکان تشخیص دقیق نقصهای میتوکندری را فراهم میکند و اطلاعات ارزشمندی را برای تنظیم خانواده فراهم میکند. دانستن جهشهای ژنتیکی که باعث بیماری میتوکندری میشوند، امکان ایجاد درمانهایی را فراهم میکند که به طور خاص هدف قرار میگیرند.
دانشمندان امیدوارند از طریق درک بهتر زیست شناسی میتوکندری، رویکردهای منحصر به فردی برای درمان بیماری های میتوکندری ایجاد کنند. از آنجا که افراد مبتلا به بیماری میتوکندری اغلب ترکیبی از میتوکندری های سالم و جهش یافته در سلول های خود دارند، درمان موثر می تواند شامل کنترل میتوکندری سالم باشد. میتوکندری های جهش یافته را میتوان تحریک کرد تا با میتوکندری سالم ترکیب شود. رویکرد دیگر ممکن است تحریک تولد میتوکندریهای جدید باشد و میتدکندری سالم را تشویق به تکثیر و پیشی گرفتن از جهشیافتهها کند.
https://www.ninds.nih.gov/health-information/disorders/mitochondrial-myopathies?fbclid=IwAR1MFQ9IeicCMAIVw5R4_4QECSn71cM-ISoEDBkkYoPlUH0vAuaBBl7u6g0#:~:text=Mitochondrial%20diseases%20that%20cause%20prominent,encephalo%20refers%20to%20the%20brain
آدرس مطب : اصفهان ، خیابان آمادگاه ، روبروی داروخانه سپاهان ، مجتمع اطبا ، طبقه اول
تلفن : 32223328 - 031