آیا آلزایمر و فراموشی در پیری یک فرایند حتمی است و یا قابل پیشگیری میباشد؟
پیرو مقاله ی قبلی در مورد خود فرایند پیری و روش های نوین سلولی مولکولی برای برعکس کردن آن، این مقاله در مورد آلزایمر و تلاش ها و روش های جدید سلولی مولکولی، برای مهار آن، ارائه میشود.
بدن به عنوان محیطی است- که مورد استفاده ی ژنها قرار میگیرد و تحت مدیریت آن است تا ژن از طریق این بدن بتواند به اهداف خود برسد.
قدرت انسان در دستکاری ژنها و محصولات پروتئینی آن، به او توان میدهد در برابر ضعف های موجود در بدن، طرح های نوینی ارائه دهد. از جمله ی این ضعف ها کاهش قدرت حافظه با افزایش سن است که گاهی به آلزایمر منجر میشود. دستاوردهای جدید علوم سلولی مولکولی، میتواند از این کاهش حافظه بکاهد.
چالش بزرگ این روش های نوین، ناتوانی آن در نگاهی همه جانبه بر انسان است. فراموشی یک چالش است ولی هر حافظه و انباشت اطلاعات، نیازمند صرف انرژی است. در سنین بالا قدرت جمع آوری انرژی، کاهش می یابد زیرا اندام های بدن فرسوده میشود؛ از این رو تلاش برای صرفه جویی در مصرف انرژی، حیاتی است. فراموشی بخشی از این صرفه جویی انرژی و صرف انرژی در اندام های حیاتی تر مانند قلب و ریه و کلیه است. ایجاد این توازن در مصرف و صرفه جویی انرژی همیشه باید در کنار تلاش های اندیشمندان در افزایش توانمندی ها به خصوص در افراد مسن مورد توجه قرار بگیرد.
یک پروتئین جدید، ممکن است به عنوان یک درمان بالقوه برای آلزایمر باشد.
13 آوریل 2023
خلاصه: محققان می گویند پپتیدی- که نسخه ی بیش فعال آنزیم CDK5 را مسدود می کند- تخریب عصبی و آسیب DNA را در مدل های موش مبتلا به بیماری آلزایمر کاهش می دهد. حیوانات تحت درمان با پپتید، توانایی بهبود یافته ای برای انجام وظایف یادگیری نشان دادند.
دانشمندان علوم اعصاب MIT راهی برای معکوس کردن تخریب عصبی و سایر علائم بیماری آلزایمر یافته اند و این با مداخله بر آنزیمی است که معمولاً در مغز بیماران آلزایمر بیش فعال است.
هنگامی که محققان موش ها را با پپتیدی درمان کردند- که نسخه ی بیش فعال آنزیمی به نام CDK5 را مسدود می کند- کاهش چشمگیری در تخریب عصبی و آسیب DNA در مغز مشاهده کردند. این موش ها همچنین بهبودهایی در توانایی خود در انجام وظایفی مانند یادگیری جهت یابی در پیچ و خم آبی نشان دادند.
لی-هوی تسای، مدیر مؤسسه یادگیری و حافظه Picower MIT و نویسنده ی ارشد این مطالعه، میگوید: «ما دریافتیم که تأثیر این پپتید قابل توجه است. ما اثرات شگفت انگیزی را از نظر کاهش واکنش های عصبی و التهابی و حتی بهبود نقایص رفتاری دیدیم.
با آزمایش های بیشتر، محققان امیدوارند که این پپتید در نهایت بتواند به عنوان درمانی برای بیماران مبتلا به بیماری آلزایمر و سایر انواع زوال عقل- که دارای بیش فعال سازی CDK5 هستند- استفاده شود.
این پپتید با CDK1، یک آنزیم ضروری که از نظر ساختاری شبیه CDK5 است، تداخلی ندارد و از نظر اندازه شبیه به سایر داروهای پپتیدی است که در کاربردهای بالینی استفاده می شود.
پینگ چیه پائو، دانشمند تحقیقاتی موسسه Picower، نویسنده اصلی مقاله است که این هفته در مجموعه مقالات آکادمی ملی علوم منتشر می شود.
تسای از اوایل دوران حرفه ای خود، نقش CDK5 را در بیماری آلزایمر و سایر بیماری های نورودژنراتیو مطالعه کرده است. او به عنوان یک دکترا، ژن CDK5 را شناسایی و شبیهسازی کرد. این ژن، نوعی آنزیم به نام کیناز وابسته به سیکلین را کد میکند. بسیاری از کینازهای وابسته به سیکلین در کنترل تقسیم سلولی نقش دارند، اما CDK5 اینطور نیست. در عوض، نقش مهمی در رشد سیستم عصبی مرکزی دارد و همچنین به تنظیم عملکرد سیناپسی کمک می کند.
CDK5
توسط پروتئین کوچکتری که با آن تعامل دارد فعال می شود. این پروتئین به نام P35، شناخته می شود. وقتی P35 به CDK5 متصل میشود، ساختار آنزیم تغییر میکند و به آن اجازه میدهد تا هدف خود را فسفریله کند- یعنی یک مولکول فسفات را به آن اضافه کند. با این حال، در آلزایمر و سایر بیماریهای عصبی، P35 به پروتئین کوچکتری به نام P25 تقسیم میشود که میتواند به CDK5 نیز متصل شود، اما نیمه عمر بیشتری نسبت به P35 دارد.
هنگامی که CDK5 به P25 متصل می شود، CDK5 در سلول ها فعال تر می شود. P25 همچنین به CDK5 اجازه می دهد تا مولکول های غیر از اهداف معمول خود از جمله پروتئین Tau را فسفریله کند.
پروتئینهای تاو هیپرفسفریلهشده، پیچهای عصبی فیبریلاری را تشکیل میدهند که یکی از ویژگیهای بارز بیماری آلزایمر است.
در کار قبلی، آزمایشگاه Tsai نشان داده است که موش های تراریخته مهندسی شده برای بیان P25 دچار تخریب شدید عصبی می شوند.
در انسان، P25 با چندین بیماری مرتبط است: آلزایمر، بیماری پارکینسون و زوال عقل فرونتوتمپورال.
دکتر سید سلمان فاطمی . نورولوژیست, [4/21/2023 1:14 AM]
شرکت های داروسازی سعی کرده اند P25 را با داروهای مولکول کوچک مورد هدف قرار دهند، اما این داروها معمولاً عوارض جانبی ایجاد می کنند زیرا با سایر کینازهای وابسته به سیکلین نیز تداخل دارند، بنابراین هیچ یک از آنها روی بیماران آزمایش نشده است.
تیم MIT تصمیم گرفت با استفاده از یک پپتید به جای یک مولکول کوچک، رویکرد متفاوتی برای هدف قرار دادن P25 اتخاذ کند. آنها پپتید خود را با دنباله ای مشابه با قطعه ای از CDK5، معروف به حلقه T طراحی کردند که ساختاری مهم برای اتصال CDK5 به P25 است. کل پپتید تنها 12 اسید آمینه، کمی طولانی تر از بسیاری از داروهای پپتیدی موجود که 5 تا 10 اسید آمینه طول دارند.
Tsai
میگوید: «از دیدگاه داروهای پپتیدی، معمولاً داروهای کوچکتر بهتر است. پپتید ما تقریباً در اندازه مولکولی ایده آل است.
جلوه های دراماتیک
در آزمایشات روی سلول های عصبی رشد یافته در یک ظرف آزمایشگاهی، محققان دریافتند که درمان با این پپتید منجر به کاهش متوسط در فعالیت CDK5 می شود. این آزمایشها همچنین نشان دادند که پپتید، کمپلکس CDK5-P35 طبیعی را مهار نمیکند و بر دیگر کینازهای وابسته به سیکلین، تأثیر نمیگذارد.
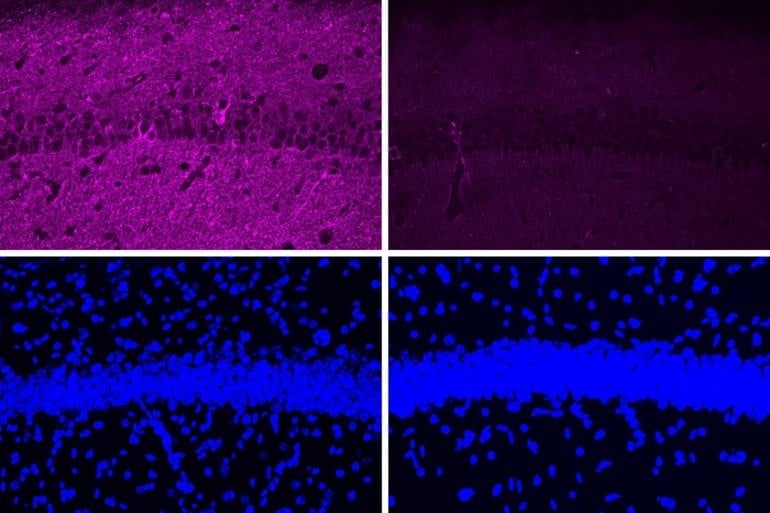
در مغز موشهایی- که با پپتید جدید، درمان شدهاند- پروتئینهای Tau بسیار کمتری دیده میشوند. پانلهای سمت چپ، نورونهای موشهایی را نشان میدهند که با یک نسخه درهم از پپتید درمان شدهاند. در دو پانل پایینی، DNA در هسته ی سلول به رنگ آبی رنگ آمیزی شده است و این، نشان می دهد تغییرات در سطوح Tau ناشی از تغییرات قابل توجهی در جمعیت سلولی نیست.
هنگامی که محققان این پپتید را در یک مدل موش مبتلا به بیماری آلزایمر- که دارای CDK5 بیش فعال است- آزمایش کردند، تعداد بیشماری از اثرات مفید از جمله کاهش آسیب DNA، التهاب عصبی و از دست دادن نورون را مشاهده کردند. این اثرات در مطالعات موش بسیار بیشتر از آزمایشات روی سلول های کشت شده بود.
درمان پپتیدی همچنین در مدل موش های آلزایمری که دارای شکل جهش یافته ای از پروتئین Tau است و منجر به گره خوردن نوروفیبریلاری می شود، پیشرفت های چشمگیری ایجاد کرد.
پس از درمان، آن موش ها کاهش در آسیب شناسی تاو و از دست دادن نورون را نشان دادند.
همراه با این اثرات در مغز، محققان بهبودهای رفتاری را نیز مشاهده کردند.
موش های تحت درمان با پپتید در کاری- که نیازمند یادگیری و جهت یابی در پیچ و خم آبی است و به حافظه فضایی متکی است- بسیار بهتر از موش هایی که با یک پپتید کنترل (نسخه ی درهم از پپتید که برای مهار CDK5-P25 استفاده می شود) درمان شده بودند، عمل کردند.
در آن مطالعات روی موش، محققان این پپتید را تزریق کردند و دریافتند که می تواند از سد خونی مغزی عبور کند و به نورون های هیپوکامپ و سایر قسمت های مغز برسد.
محققان همچنین تغییرات بیان ژن را که در نورون های موش پس از درمان با پپتید رخ می دهد، تجزیه و تحلیل کردند.
از جمله تغییراتی که آنها مشاهده کردند، افزایش بیان حدود 20 ژن بود که معمولاً توسط خانواده ای از تنظیم کننده های ژن به نام MEF2 فعال می شوند.
آزمایشگاه Tsai قبلاً نشان داده بود که فعالسازی MEF2 این ژنها میتواند انعطافپذیری را در برابر اختلالات شناختی در مغز افراد مبتلا به تاو ایجاد کند. او فرض میکند که درمان پپتیدی ممکن است اثرات مشابهی داشته باشد.
Tsai
اکنون قصد دارد مطالعات بیشتری را در مدلهای دیگر بیماریهای موش انجام دهد که شامل تخریب عصبی مرتبط با P25 میشود، مانند زوال عقل فرونتومپورال، زوال عقل ناشی از HIV و اختلالات شناختی مرتبط با دیابت.
او میگوید: «بسیار سخت است که دقیقاً بگوییم کدام بیماری بیشترین سود را خواهد داشت، بنابراین فکر میکنم کار بسیار بیشتری لازم است.
عنوان مقاله:
یک پپتید مشتق شده از Cdk5، فعالیت Cdk5/p25 را مهار می کند و فنوتیپ های عصبی را بهبود می بخشد توسط Li-Huei Tsai و همکاران. PNAS
خلاصه ی مقاله:
یک پپتید مشتق شده از Cdk5، فعالیت Cdk5/p25 را مهار می کند و فنوتیپ های عصبی را بهبود می بخشد.
فعالیت نابجای کیناز وابسته به سیکلین (Cdk5) در بیماریهای نورودژنراتیو مختلف نقش دارد. این اثر مضر با شکاف پاتولوژیک فعال کننده Cdk5 p35 به محصول کوتاه شده p25 انجام می شود که منجر به فعال سازی طولانی مدت Cdk5 و تغییر ویژگی بستر می شود.
افزایش سطح p25 در انسان و جوندگان مبتلا به تخریب عصبی، گزارش شده است، و مزیت مسدود کردن ژنتیکی تولید p25 قبلاً در مدلهای تخریبکننده عصبی جوندگان و انسان نشان داده شده است.
دکتر سید سلمان فاطمی . نورولوژیست, [4/21/2023 1:14 AM]
در اینجا، ما یک قطعه ی پپتید طولانی 12 آمینو اسید مشتق شده از Cdk5 (Cdk5i) را گزارش می کنیم که به طور قابل توجهی کوچکتر از مهارکننده های پپتید موجود در Cdk5 (P5 و CIP) است اما میل اتصال بالایی را نسبت به کمپلکس Cdk5/p25 نشان می دهد و برهمکنش را مختل می کند و فعالیت کیناز Cdk5/p25 را کاهش می دهد.
پپتید Cdk5i-FT هنگامی که با یک فلوروفور (FITC) و توالی ترانس فعال کننده رونویسی (TAT) نافذ به سلول، برچسب گذاری و تگ می شود، ویژگی هایی برای نفوذ بهتر سلولی و مغزی را نشان می دهد و در برابر فنوتیپ های عصبی مرتبط با بیش فعالی مدل Cdk5 در سلول و سلول محافظت می کند. تخریب عصبی، پتانسیل درمانی Cdk5i را برجسته می کند. https://neurosciencenews.com/alzheimers-peptide-23002/
آدرس مطب : اصفهان ، خیابان آمادگاه ، روبروی داروخانه سپاهان ، مجتمع اطبا ، طبقه اول
تلفن : 32223328 - 031