درمان با سلول های بنیادی مزانشیمی در بیماران اسکلروز آمیوتروفیک جانبی بررسی جامع اطلاعات بیماری و دیدگاه های آینده
خلاصه
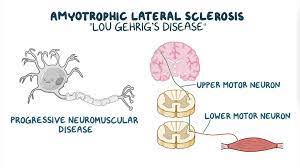
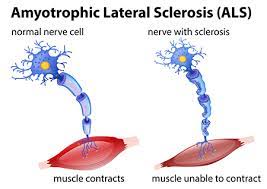
اسکلروز جانبی آمیوتروفیک (ALS) یک بیماری نادر عصبی پیشرونده و کشنده است که در درجه اول نورون های حرکتی فوقانی و تحتانی را با میزان بروز سالانه 0.6 تا 3.8 در هر 100000 نفر درگیر می کند.
ضعیف شدن و آتروفی تدریجی عضلات ارادی اولین نشانه ی شروع بیماری است که بر تمام جنبه های زندگی بیماران از جمله خوردن، صحبت کردن، حرکت و حتی تنفس تاثیر می گذارد.فقط 10-5 درصد از بیماران، دارای نوع خانوادگی بیماری هستند و الگوی اتوزومال غالب را نشان می دهند، اما علت بیماری در 90 درصد بیماران، ناشناخته است (اسپورادیک ALS).
اما در هر دو نوع بیماری، بقای بیمار 2 تا 5 سال از شروع بیماری است.برخی از نشانگرهای زیستی بالینی و مولکولی، تصویربرداری رزونانس مغناطیسی (MRI)، آزمایش خون یا ادرار، بیوپسی عضلانی و آزمایش ژنتیکی روشهای تکمیلی برای تشخیص بیماری هستند.در این راستا، استفاده از سلولهای بنیادی مزانشیمی (MSCs) برای درمان یا مدیریت بیماری، سالهاست که در مطالعات پیش بالینی و بالینی رایج بوده است.سلولهای بنیادی مزانشیمی سلولهای چند توانی هستند که دارای قابلیت تنظیم ایمنی، ضدالتهابی و تمایز هستند که آنها را کاندید خوبی برای این منظور میکند.
هدف این مقاله ی مروری، بحث در مورد جنبههای مختلف بیماری ALS و تمرکز بر نقش سلولهای بنیادی مزانشیمی در مدیریت بیماری بر اساس کارآزماییهای بالینی انجام شده است.
معرفی
این اختلال برای اولین بار توسط ژان مارتین شارکو در سال 1869 به عنوان یک اختلال عصبی حرکتی خاص توصیف شد (2و معمولاً به دلیل بازنشستگی این بازیکن مشهور در دهه 1940 با این بیماری به عنوان بیماری لو گریگ شناخته می شود (3 ).به دلیل ماهیت پیشرونده ALS، علائم با گذشت زمان شدیدتر می شوند (4 ).در واقع، شروع بیماری معمولاً بسیار نامحسوس است، اما به تدریج علائم به ضعف یا آتروفی قابل لمس تبدیل میشوند (5
علائم اولیه شامل درگیری عضلانی پرش (مانند بازو، پا، شانه یا زبان)، سفتی عضلانی (اسپاستیسیته)، اسپاسم عضلانی و مشکلات بلع است (6 ،7 .این علائم در ابتدا کانونی هستند، اما با پیشرفت بیماری، تمایل به گسترش در سراسر بدن دارند (5 که معمولاً منجر به اشکال در بلع (دیسفاژی)، مشکل گفتار (دیس آرتری) و اختلال تنفس (تنگی نفس) میشود (8 .در این زمینه، اختلال عملکرد عضلات تنفسی علت اصلی مرگ در بیماران ALS طی 3 تا 5 سال پس از شروع علائم است (5
راهبردهای درمانی جدید می تواند نویدبخش افزایش طول عمر بیمار ALS باشد.رفتار مهاجرتی، اثر بازسازی بافت (12 و توانایی تمایز به انواع سلولهای مختلف مانند سلولهای عصبی (15 ، سلولهای بنیادی مزانشیمی را کاندیدای مناسبی در این زمینه کرده است.
عوامل دخیل در توسعه ALS
تا به امروز، علت ALS ناشناخته است و این معمای بی پاسخ برای محققان باقی مانده است.با این حال، شواهد علمی وجود دارد که هم ژنتیک و هم محیط، بازیگران کلیدی این سناریو هستند (16) به شرح زیر:
ژنتیک
تحقیقات نشان می دهد که برخی جهش های ژنی خاص (بیش از 30 ژن مختلف) با تخریب نورون حرکتی و توسعه ALS مرتبط هستند (17 ).برخی از این جهشها مستقیماً مسئول القای بیماری هستند زیرا از والدین دارای فرزندان بیمار به ارث میرسند و به عنوان ژنهای ALS خانوادگی جهش یافته از جمله SOD1، TARDBP، FUS، OPTN، VCP، UBQLN2، C9ORF72، ANG، SETX و SQSTM1 شناخته میشوند.18
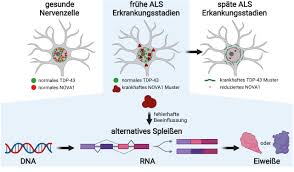
فاکتورهای محیطی
بسیاری از مطالعات اپیدمیولوژیک عوامل محیطی دخیل در ایجاد ALS را بررسی کرده اند (20 ،21 ).نتایج بهدستآمده نشان میدهد که سبک زندگی نامناسب و عوامل محیطی مختلف ممکن است بر شروع و گسترش بیماری تأثیر بگذارد، از جمله قرار گرفتن در معرض سموم، فلزات سنگین، آفتکشها، مواد شیمیایی کشاورزی، میدانهای مغناطیسی الکتریکی و ویروسها (22-24)
همچنین فعالیت بدنی، ضربه بدنی، رژیم غذایی، سیگار کشیدن، خطرات شغلی، منطقه جغرافیایی، (کمپلکس دمانس ALS/پارکینسون)، سن و جنسیت مرد از دیگر عوامل محیطی تاثیرگذار در نظر گرفته می شوند( 25-28)
تشخیص
تشخیص ALS عمدتاً بر اساس تظاهرات بالینی است که نارسایی نورون حرکتی فوقانی و تحتانی را نشان میدهد و آزمایش منفرد خاصی برای تشخیص آن وجود ندارد ).همچنین، از آنجایی که این بیماری می تواند شرایط سایر بیماری های عصبی را تقلید کند، تشخیص آن در مراحل اولیه دشوار و گاهی غیرممکن است (30 .برخی از آزمایشهای رایج برای تشخیص از سایر بیماریهای عصبی عبارتند از: مطالعه هدایت عصبی (NCS)، تصویربرداری تشدید مغناطیسی (MRI)، آزمایشهای خون و ادرار، الکترومیوگرام (EMG)، بیوپسی عضلانی و آزمایش ژنتیک، (31)سابقه درد قابل توجه بیمار یا آتروفی عضلانی، تست اسپیرومتری، آزمایشگاه تصویربرداری عصبی، و آزمایش الکترودیاگنوستیک می تواند در تشخیص بیماری بسیار مفید باشد (32).امروزه، یکی دیگر از روش های پیشنهادی مکمل برای تشخیص بیماری، استفاده از بیومارکرهای بالینی و مولکولی است (22 )
نشانگرهای زیستی ALS
فقدان یک روش تشخیصی قطعی برای ALS و در نتیجه پیشرفت سریع بیماری به دلیل تاخیر در تشخیص، نیاز به کشف راه حل های تشخیصی جدید را برجسته می کند.در این راستا، بیومارکرهای بالینی و مولکولی مختلفی با نقش های تشخیصی حیاتی وجود دارد (34
برخی از مهمترین آنها الکترومیوگرافی (برای تشخیص آسیب نورون حرکتی)، تحریک مغناطیسی ترانس کرانیال (یکپارچگی عملکردی نورون ها)، میوگرافی امپدانس الکتریکی (یکپارچگی عملکردی و ساختار عضلانی) و رویکردهای فیزیولوژیک عصبی (35 ،36) هستند.همچنین، بیومارکرهای مولکولی مانند سایتوکاینهای التهابی کمککنندههای کلیدی در این سناریو هستند و میتوانند در مایعات بدن از جمله CSF، ادرار، خون و بزاق شناسایی شوند (35 ،37)
این بیومارکرها را می توان به صورت زیر دسته بندی کرد: نشانگرهای زیستی مربوط به سمیت تحریکی، استرس اکسیداتیو، التهاب، اختلال عملکرد متابولیک، تخریب عصبی و سایر نشانگرهای زیستی خون ،38
برخی از رایج ترین مکانیسم های بیماریزای پیشنهادی عبارتند از: اختلال در متابولیسم RNA، اختلال در هموستاز پروتئین، نقص در حمل و نقل نوکلئوسیتوپلاسمی، اختلال در ترمیم DNA، سمیت تحریکی، اختلال عملکرد میتوکندری، استرس اکسیداتیو، اختلال در حمل و نقل آکسونی، التهاب رگهای عصبی، التهاب رگهای عصبی، نقص، و تغییر در حمل و نقل نوکلئوسیتوپلاسمی (56 ،58 )
استراتژی های درمانی فعلی
پیچیدگی آسیب شناسی ALS، از مکانیسم های مولکولی تا علائم بالینی، شناسایی عامل ایجادکننده دقیق را دشوار می کند و توسعه یک دارو یا درمان هدفمند را دشوار می کند. از سوی دیگر، متأسفانه علیرغم شیوع روزافزون این بیماری به دنبال صنعتی شدن بیشتر کشورها در دهه های اخیر (که شانس قرار گرفتن در معرض عوامل خطر محیطی را افزایش می دهد) و تلاش محققان، هنوز درمان قطعی برای ALS وجود ندارد. (59)با این حال، در اکثر جوامع اروپایی، ریلوزول (سانوفی آونتیس، ایالات متحده آمریکا) به عنوان یک داروی ضد گلوتامات (50 میلی گرم دو بار در روز) به عنوان تنها داروی تایید شده در مدیریت بیماری استفاده می شود، اما اثرات نامطلوبی مانند مشکلات کبدی و اسهال و اسهال دارد ولی در بهترین حالت می تواند میانگین امید به زندگی بیماران را بین 3 تا 6 ماه افزایش دهد (9و60). همچنین، داروهای آنتی اکسیدانی امروزه به دلیل نقش مهم استرس اکسیداتیو در القا و/یا پیشرفت ALS مورد توجه بسیاری از محققان قرار گرفته است (56)یکی از رایج ترین داروهای آنتی اکسیدانی در این زمینه Edaravone است (Mitsubishi Tanabe Pharma Corporation (MTPC)، ایالات متحده آمریکا) و ایمنی و اثربخشی آن اخیراً در چندین کارآزمایی بالینی مورد مطالعه قرار گرفته است(61-63 ). در این راستا، تجزیه و تحلیل نتایج درمان 2 ساله بیماران ALS با اداراوون بر روی 621 بیمار ALS (331 بیمار در گروه مداخله و 290 بیمار در گروه کنترل) نشان داد که این دارو به خوبی توسط بیماران تحمل می شود، اما تأثیر معنی داری بر بیماری ندارد. پیشرفت و عملکرد تنفسی گزارش شد (64 ). با این حال، در مطالعه دیگری روی 22 بیمار ALS در کره، استفاده از Edaravone تأثیر متوسطی بر امتیاز ALSFRS و FVC در بیماران نشان داد. اگرچه هنوز در نتایج بهدستآمده در این زمینه تناقض وجود دارد، امروزه Edaravone به عنوان یک داروی مورد تایید برای کاهش پیشرفت ALS در ایالات متحده آمریکا، ژاپن، کانادا، کره جنوبی و سوئیس پذیرفته شده است (5)

سایر راهکارهای درمانی پیشنهادی
علاوه بر درمانهای دارویی ذکر شده در بالا، برخی روشهای درمانی دیگر نیز برای کنترل و کاهش علائم بیماری پیشنهاد شدهاند، از جمله حمایت تنفسی (65 )، حمایت روانی و اجتماعی (66)، کاردرمانی (67 )، گفتار درمانی (68) . و فیزیوتراپی (69 ). همچنین استفاده از فاکتورهای تغذیه ای با توجه به نقش کلیدی آنها در بقا و نگهداری نورون های حرکتی، به عنوان جایگزین های درمانی بالقوه در بیماری ALS پیشنهاد شده است. اگرچه، متأسفانه، انفوزیون زیر جلدی برای برخی از این عوامل تغذیهای مانند CNTF و IGF-1 در مطالعات کارآزمایی بالینی منجر به مزایای درمانی قابل توجهی نشده است (70)، اما تزریق داخل نخاعی (IGF-1 و BDNF) نتایج بهبود متوسطی را در برخی از آنها نشان داده است. موارد بدون عوارض جانبی شدید (49)که بیانگر نیاز به انجام بیشتر مطالعات حیوانی و انسانی در این زمینه است.
تغییرات ژنتیکی مانند استفاده از RNA خاموش کننده ژن های جهش یافته SOD1 یا TARDBP، ALS2 و ALS4 در بیماران خانوادگی ALS می تواند به عنوان یک روش درمانی اختیاری خوب در نظر گرفته شود (71 )). طراحی مولکول های چند منظوره جمع کننده ی آهن مانند M30 و HLA20، به تنهایی یا در ترکیب با سایر ترکیبات، رویکرد ارزشمند دیگری برای ارتقای بقای اعصاب حرکتی از طریق اثرات حمایتی بر تمایز عصبی و جوانه زدن آکسون ها است که منجر به عصب دهی مجدد فیبرهای عضلانی می شود (72)
روش رایج دیگری که از گذشته تا به امروز برای درمان بیماران ALS یا کاهش سرعت پیشرفت بیماری در مطالعات پیش بالینی و بالینی استفاده شده است، استفاده از سلول های بنیادی مزانشیمی است (که در ادامه با جزئیات بیشتر توضیح داده شده است) (12،73)
سلول های بنیادی مزانشیمی (MSCs) و نقش آنها در بهبود ALS
سلول های بنیادی مزانشیمی سلول های چند توان استرومایی بالغ هستند که برای اولین بار در سال 1976 توسط Friedenstein و همکاراناز مغز استخوان (BM) به عنوان واحدهای تشکیل دهنده کلنی فیبروبلاستیک جداسازی شدند.و بعداً در بسیاری از بافت های دیگر شناسایی شد (74). در بدن انسان، آنها تا زمانی که سیگنالی برای تبدیل شدن به یک سلول تخصصی با عملکردهای سلولی تخصصی جدید دریافت نکنند، متعهد نمی مانند (75 ). در بسیاری از بافت ها، آنها به عنوان یک مخزن داخلی عمل می کنند و همچنین برای رشد، تکامل، بقا و ترمیم و ساخت قسمت های مختلف بدن ضروری هستند (76). سلول های بنیادی مزانشیمی در همه ارگانیسم های چند سلولی یافت می شوند و باید بر اساس دستورالعمل انجمن بین المللی سلول درمانی (ISCT) سه ویژگی اساسی را از خود نشان دهند. اولاً، تکثیر با تقسیم سلولی میتوزی برای تولید سلول ها همانند سلول مبدا است (76 ) دوم، MSCها باید بتوانند خود را در دوره های طولانی تجدید کنند (77 ). سوم، آنها دارای توانایی پرتوان برای تمایز به چندین دودمان مختلف (به عنوان مثال، استئوسیت ها، آدیپوسیت ها و غضروفی ها) تحت شرایط فیزیولوژیکی خاص هستند (14،78)
آنها به راحتی قابل دسترسی هستند و می توانند از دو نوع سلول جدا شوند: منابع بالغ مانند BM (79 بافت چربی (80 ، خون محیطی (81 ، و غیره، و منابع جنینی مانند غشای آمنیوتیک (82)، جفت (83) و بند ناف (84 ). تا به امروز، این سلول ها و مشتقات آنها در درمان بیماری های مختلف و بسیاری از آزمایشات بالینی، از جمله دیابت، کووید-19 (86 ) و همچنین بیماری های تخریب کننده عصبی مانند آلزایمر (90ALS (12 و آتاکسی (91 ) و بیماری پارکینسون (92)استفاده شده اند.
این سلول ها دارای چندین ویژگی برجسته هستند که آنها را کاندید مناسبی برای درمان بیماری ها می کند، از جمله: (1) آنها با ملاحظات اخلاقی مرتبط با استفاده از سلول های بنیادی جنینی (ESCs) مواجه نیستند (93)، (2) می توان آنها را جدا کرد. و همدر شرایط آزمایشگاهیو همدر داخل بدنبا استفاده از یک روش ساده گسترش یافته اند (14) ،94 )، (3) دارای خواص متعدد تعدیل کننده ایمنی و ضد آپوپتوز از طریق مکانیسم های مختلف هستند (95،96)، (4) زمان محدود تکثیر آنها امکان کاهش تبدیل بدخیم پس از انفوزیون در مقایسه با ESCs و iPSCs (97 (5) ایمنی زا نیستند و به دلیل عدم بیان MHCs با توجه به امکان پیوند اتولوگ (98)و همچنین دارای رفتار مهاجرتی هستند و می توانند قبل از تزریق نیازی به مصرف داروی سرکوب کننده سیستم ایمنی ندارند.خطوط سلولی متعدد مانند تمایز BM-MSCs (15 و کوریون-MSCs به سلولهای شبه نورون حرکتی عملکردی. نقش طلایی سلول های بنیادی مزانشیمی در بیماری های عصبی مانند ALS به دلیل نقش آن ها در تمایز به سلول های عصبی و جایگزینی سلول های مرده و آسیب دیده با سلول های عملکردی جدید است. همچنین با ترشح عوامل تغذیهای و حذف مولکولهای سمی به بهبود محیط اطراف نورونها کمک میکنند و نقش محافظتی برای نورونها دارند. (12). ترمیم توالی های عصبی آسیب دیده مانند دندریت ها و آکسون ها و تحریک مسیرهای مغزی جایگزین برای بهبود حرکت و هماهنگی از دیگر مکانیسم های موثر این سلول ها در درمان بیماران ALS است (98 ). همه این ویژگی های درخشان، سلول های بنیادی مزانشیمی را به منبع خوبی برای سلول درمانی و پزشکی بازساختی تبدیل می کند.شکل 2 )به طور شماتیک برخی از اثرات سلول های بنیادی مزانشیمی بر ترمیم نورون ها در بیماران ALS را نشان می دهد.
مطالعات پیش بالینی با استفاده از سلول های بنیادی مزانشیمی در مدل های ALS
مکانیسم های پیشنهادی ترمیم عصبی توسط سلول های بنیادی مزانشیمی
سلولهای بنیادی مزانشیمی (MSCs) سیتوکینهای مختلف ترشح میکنند و فاکتورهای رشد از جمله فاکتورهای نوروتروفیک مانند فاکتور رشد تبدیلکننده (TGF)-1 و فاکتور رشد اندوتلیال عروقی (VEGF) به محافظت درمانی از نورونها کمک میکنند، رشد نورون درونزا، نوروژنز و رگزایی را تقویت میکنند. تقویت اتصال سیناپسی و میلیناسیون مجدد آکسون های آسیب دیده، کاهش آپوپتوز و تنظیم التهاب عمدتاً از طریق اقدامات پاراکرین.
مطالعات پیش بالینی با استفاده از سلول های بنیادی مزانشیمی در مدل های ALS
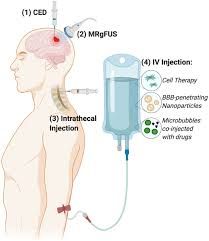
تحقیقات پیش بالینی که علل و درمانهای بالقوه ALS را بررسی میکند، اساساً بر مدلهای جوندگان و موش متکی است که ژنهای SOD1 انسانی جهشیافته را بیش از حد بیان میکنند و الگوهای مشابهی از آسیبشناسی و پیشرفت بیماری را با آنچه در انسان مشاهده میشود نشان میدهند (100). با استفاده از این مدلها، محققان دریافتهاند که پیوند سلولهای بنیادی مزانشیمی از طریق مسیرهای مختلف مانند داخل نخاعی (IT)، داخل وریدی (IV)، عضلانی (IM) و داخل مغزی (IC) میتواند یک رویکرد ایمن و موثر در به تاخیر انداختن این بیماری و کاهش عملکرد حرکتی و ترویج نوروژنز (101 )باشد.
همچنین اعتقاد بر این است که ترشح عوامل مختلف مانند سایتوکین ها و فاکتورهای رشد مانند TGF-1 و VEGF به محافظت درمانی نورون ها و کاهش التهاب پس از پیوند کمک می کند (102 ). علاوه بر این، مطالعات مربوط به تجویز سیستماتیک یا درون نخاعی سلول های بنیادی مزانشیمی از BM یا بافت چربی بر روی جوندگان جهش یافته، مزایای قابل توجهی را از نظر به تاخیر انداختن انحطاط نورون های حرکتی، بهبود عملکرد حرکتی و افزایش طول عمر نشان داده است (73)
مطالعه ای تأثیر تزریق ترکیبی داخل نخاعی و سیستمیک سلول های بنیادی مزانشیمی را در موش های تراریخته علامت دار SOD-G93A بررسی کرد. نتایج نشان داد که پیوند MSC تأثیر قابلتوجهی بر فعالیت حرکتی، قدرت گرفتن و طول عمر دارد و منجر به تعداد بیشتری از نورونهای حرکتی با اندازه بزرگتر با آپوپتوز کمتر شد
تحقیقات دیگری نشان داد که تزریق داخل وریدی سلول های بنیادی مزانشیمی در موش های SOD1 تأثیر قابل توجهی بر طولانی شدن بقا و کاهش علائم، همراه با بهبود پارامترهای بافت شناسی و بیوشیمیایی متعدد داشت (105)
این آزمایشات موفقیت آمیز منجر به این باور شده است که درمان ALS با سلول های بنیادی مزانشیمی می تواند خواص محافظت کننده عصبی یا بازسازی کننده عصبی را که عملکردهای بیولوژیکی را تعدیل می کند، بهبود بخشد (106)
همانطور که نتایج مطالعات فوق نشان می دهد، استفاده از سلول های بنیادی مزانشیمی در مدل های حیوانی ALS نتایج موثری را نشان داده است. تأخیر در اختلال عملکرد حرکتی و افزایش طول عمر نتایج امیدوارکنندهای است که میتواند با مکانیسمهای مختلف عملکرد سلولهای بنیادی مزانشیمی، از جمله ویژگیهای ضد التهابی، ضد آپوپتوز و تنظیم ایمنی توضیح داده شود (110 )
مطالعات بالینی با استفاده از MSCها در بیماران ALS
اولین کارآزمایی بالینی که از MSCها برای ارزیابی ایمنی و قدرت آنها در درمان بیماران ALS استفاده کرد، در سال 2003 توسط Mazziniو همکارانشانجام شد . . در این مطالعه، MSCهای مغز استخوان اتولوگ حل شده در مایع مغزی نخاعی اتولوگ، به صورت داخل نخاعی به 7 بیمار ALS تزریق شد. از نظر ایمنی، این سلول ها در همه بیماران به خوبی تحمل شده و هیچ عارضه جانبی جدی مشاهده نشد. همچنین تصاویر MRI تغییرات ساختاری غیرطبیعی را در نخاع به دنبال تزریق سلول نشان نداد. با این حال، به دلیل عدم وجود گروه کنترل در این مطالعه، هیچ نتیجه ای در مورد اثربخشی سلول ها گزارش نشد، اما تحمل پذیری خوب سلول ها امید جدیدی را برای تحقیقات بیشتر در این زمینه ایجاد کرد. در یک دوره پیگیری 36 ماهه، در مطالعه دیگری توسط Mazziniو همکاران در سال 2006 یک نتیجه امیدوارکننده دیگر گزارش شد. در این مطالعه، از 9 بیمار ALS شرکت کننده، 5 بیمار کاهش قابل توجهی در ظرفیت حیاتی اجباری (FVC) و نمره ALS-FRS به دنبال تزریق سلول نشان دادند. همچنین، هیچ عارضه جانبی جدی در هیچ یک از شرکت کنندگان مشاهده نشد (112 ). در مجموع، نتایج Mazziniو همکاراننشان داد که تزریق مستقیم سلول های بنیادی مزانشیمی اتولوگ به نخاع بیماران ALS بدون هیچ گونه سمیت، به خوبی توسط بیماران قابل تحمل است (112 ). نتایج یک پیگیری طولانی مدت 9 ساله 19 بیمار ALS دریافت کننده BM-MSCهای اتولوگ را گزارش کرد. در این مطالعه، همانطور که انتظار می رفت، هیچ عارضه جانبی جدی مرتبط با تزریق سلولی مانند تشکیل تومور در هیچ یک از بیماران گزارش نشد. همچنین کاهش قابل توجهی در پیشرفت بیماری و افزایش امید به زندگی در 6 بیمار مشاهده شد . در یک کارآزمایی بالینی اکتشافی دیگر جنبه های جدیدی از خواص تنظیم کننده ایمنی سلول های بنیادی مزانشیمی ظاهر شد. آنالیز فلوسیتومتری مونوسیت های خون محیطی 5 بیمار ALS تغییرات قابل توجهی را در زیرگروه های لنفوسیت T، به دنبال تزریق داخل نخاعی و داخل وریدی سلول های بنیادی مزانشیمی نشان داد. نتایج بهدستآمده افزایش 72 درصدی در زیرمجموعههای تنظیمکننده T (سلولهای CD4+ CD25+ T) و کاهش 30 تا 60 درصدی در سلولهای CD86+، CD83+، HLADR+دندریتیک میلوئید، و سلولهای فعال CD4+ را 24 ساعت پس از پیوند سلولهای بنیادی مزانشیمی نشان داد (114
به دنبال پیشرفت علوم، تعداد آزمایشهای بالینی مرتبط با ALS در سالهای اخیر افزایش یافته است. به عنوان مثال، در یک مطالعه اخیر که توسط تیم تحقیقاتی ما روی 15 بیمار ALS انجام شد، نتایج امیدوارکنندهای مشاهده شد. در این مطالعه، 3 ماه پس از تزریق IV و IT همزمان BM-MSCs، افزایش قابل توجهی در ALS-FRS و FVC مشاهده شد. همچنین هیچ عارضه جانبی جدی در هیچ یک از بیماران مشاهده نشد (12)نتایج برخی از آزمایشات بالینی انجام شده در این زمینه را خلاصه می کند.
به طور خلاصه، ALS یک بیماری تخریب کننده عصبی کشنده است که بر تمام جنبه های سبک زندگی فرد مبتلا از جمله صحبت کردن، بلعیدن، تنفس، حرکت و بقای آنها تأثیر می گذارد. سلول های بنیادی مزانشیمی به دلیل ویژگی های درخشانشان مانند توانایی ضد التهابی، تنظیم ایمنی و تمایز، یک رویکرد درمانی خوب در نظر گرفته می شوند. بسیاری از مطالعات پیش بالینی و بالینی با استفاده از سلول های بنیادی مزانشیمی در مدیریت ALS با نتایج امیدوارکننده ای وجود دارد. هدف این مقاله جمع آوری اطلاعات کلی و داده های موجود در این زمینه است.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10329242/
آدرس مطب : اصفهان ، خیابان آمادگاه ، روبروی داروخانه سپاهان ، مجتمع اطبا ، طبقه اول
تلفن : 32223328 - 031